morfologi
Pada tingkat makroskopik, tingkat variabel atrofi kortikal (pengurangan jaringan atau massa organ) dapat diamati pada penyakit Alzheimer, ditandai dengan pembesaran alur parietal, lebih ditekankan pada lobus frontal, temporal, dan parietal. Atrofi ini dikompensasi oleh pembesaran rongga ventrikel sekunder akibat hilangnya parenkim (gambar 1). Secara khusus, pada tahap lanjut penyakit, struktur lobus temporal medial, termasuk hippocampus, korteks entorhinal dan amigdala, mengalami atropi parah, mengingat keterlibatannya mulai dari tahap awal patologi.
Selain itu, penyakit Alzheimer juga menghadirkan perubahan mikroskopis, yang dikenal sebagai plak pikun ekstraseluler dan kluster neurofibrillary intraseluler, yang mewakili dasar diagnosis histologis. Dengan perkembangan penyakit, maka, ada kehilangan saraf yang serius disertai dengan gliosis (proliferasi terbatas atau difus, sifat reaktif, sel neuroglia, yaitu, sel yang merupakan stroma pendukung jaringan saraf) di wilayah yang sama di mana keberadaan plak dan kluster neurofibrillary lebih besar.
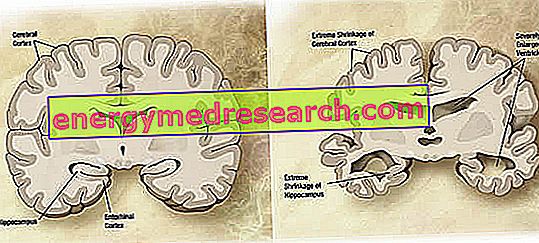
Gambar 1. Bagian otak koroner: perbedaan antara otak normal dan otak yang dipengaruhi oleh AD (sumber gambar wikipedia).
patogenesis
Penyakit Alzheimer ditandai terutama oleh dua lesi yang khas: akumulasi ekstraselular plak pikun yang terutama terdiri dari β-amiloid peptida (Aβ) dan kluster neurofibrillary intraneuronal, yang dibentuk oleh protein tau hiperfosforilasi.
- Plak pikun dapat ditemukan pada tingkat area otak seperti hippocampus, amygdala dan neocortex.
Aβ peptide berasal dari pemotongan proteolitik dari prekursor protein amiloid (APP), oleh β-sekretase. Potongan ini menghasilkan fragmen karboks terminal 99 residu (CTF atau C99) yang kemudian dipotong oleh β-sekretase untuk menghasilkan fragmen Aβ, memiliki panjang yang berbeda. Diketahui bahwa spesies yang paling melimpah dari Aβ adalah fragmen Aβ40. Fragmen lain yang diketahui terbentuk dari potongan proteolitik, kurang melimpah dari Aβ40, adalah Aβ42, lebih rentan membentuk fibril amiloid, yang terakumulasi sebagai spesies Aβ di otak seseorang dengan penyakit Alzheimer.
- Komponen lain hadir dalam penyakit Alzheimer diwakili oleh kelompok neurofibrillary yang terdiri dari kumpulan filamen hadir dalam sitoplasma neuron. Cluster neurofibrillary tidak larut dan tampaknya resisten terhadap proses proteolisis in vivo, sehingga tetap ada di bagian jaringan bahkan untuk waktu yang lama setelah kematian neuron. Mengamati struktur, gugus fibrillar terdiri dari filamen heliks ganda dan filamen linier dengan komposisi yang sama. Menganalisis komposisi, helai heliks ganda sebagian besar terbuat dari protein tau hyperphosphorylated. Tau adalah protein aksonal yang terkait dengan mikrotubulus yang memfasilitasi perakitannya.
Perubahan neuropatologis penting lainnya hadir pada penyakit Alzheimer termasuk disfungsi mitokondria, kerusakan neuron oksidatif, kehilangan sinaptik dan degenerasi aksonal.
Aspek neurokimia
Seperti yang sudah dijelaskan, peptida Aβ, berasal dari pemotongan proteolitik prekursor APP, mewakili komponen neurotoksik dari penyakit Alzheimer . Secara khusus, telah dihipotesiskan bahwa Aβ mungkin penting untuk fungsi otak normal dan, jika mengatasi konsentrasi tertentu, itu mungkin menjadi neurotoksik. Selain itu, baik agregat dan isoform yang berbeda dari Aβ dapat memiliki peran biologis, fisiologis atau patologis yang berbeda, menentukan dan berpartisipasi dalam tahap selanjutnya penyakit. Telah diamati bahwa Aβ bertindak sebagai neuromodulator, mempengaruhi pelepasan beberapa neurotransmiter tanpa adanya tanda-tanda neurotoksisitas yang jelas.
Sebagai contoh, peran neuromodulator Aβ, dalam konteks fisiologis, dapat memiliki arti penting untuk keseimbangan yang tepat dari sistem neurotransmitter. Sudah diketahui bahwa sistem ini terdiri dari neurotransmitter, zat yang menyampaikan informasi antara sel-sel yang membentuk sistem saraf, neuron, melalui transmisi sinaptik.
Dalam kondisi patologis, di sisi lain, transmisi sinaptik yang dimediasi-A dapat dikaitkan dengan perubahan neurotransmisi sebelum kejadian neurodegeneratif. Sebagai akibat dari perubahan-perubahan ini, gangguan kognitif awal dan non-kognitif dapat timbul, berdasarkan pada sistem neurotransmitter yang terpengaruh dan berbagai area otak yang terlibat.
Perubahan sistem neurotransmitter dan mekanisme transduksi sinyal pada otak individu yang menderita penyakit Alzheimer sangat kompleks. Salah satu sistem yang tampaknya diubah menyangkut sistem pensinyalan kolinergik, yang melibatkan neurotransmitter asetilkolin. Memang, telah ditunjukkan bahwa individu yang menderita penyakit Alzheimer menunjukkan penurunan transmisi kolinergik pada tingkat korteks dan hippocampus, area otak penting yang didedikasikan untuk fenomena seperti pembelajaran dan memori. Selain sistem neurotransmitter ini, perubahan dalam sistem noradrenergik, serotonergik, serta glutamat dan GABA telah diamati pada penyakit Alzheimer.



